creos™ syntogain
Sostituto biomimetico per innesto osseo per una rigenerazione efficiente.1
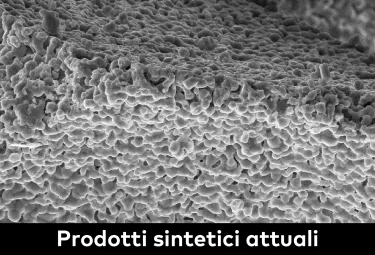
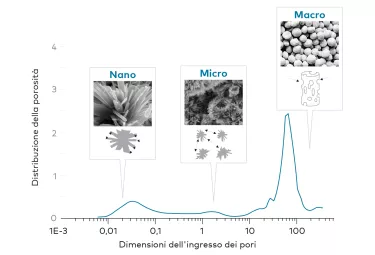
Sostituto sintetico di osso poroso biocompatibile, caratterizzato da una struttura porosa interconnessa multidirezionale, simile a quella dell'osso spongioso umano, destinato all'uso in chirurgia parodontale, orale e maxillo-facciale.
Quale aspetto fa la differenza?
creos™ syntogain appartiene alla nuova generazione di innesti ossei sintetici. Il suo processo di produzione avanzato1 in ambiente acquoso e a bassa temperatura consente di ottenere un innesto osseo con tratti distintivi chiave.
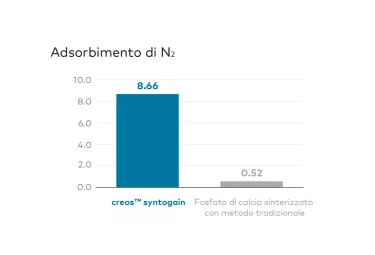
COMPOSIZIONE ESCLUSIVA DEL MATERIALE1,7,8
80% di idrossiapatite carente di calcio (CDHA) e 20% di BTCP (beta-fosfato tricalcico).
Processo di produzione avanzato1
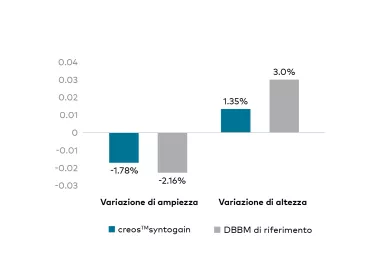
creos™ syntogain ha dimostrato non inferiorità rispetto alla DBBM di riferimento in termini di conservazione dimensionale della cresta alveolare
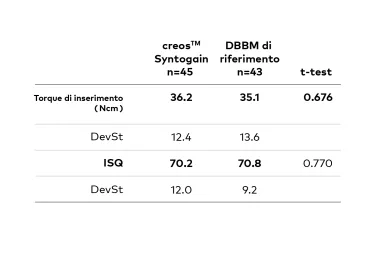
In uno dei più estesi studi clinici randomizzati (RCT) eseguiti sulla rigenerazione ossea dentale15, 102 pazienti sono stati randomizzati per ricevere un trattamento di aumento osseo con creos syntogain o con la matrice ossea bovina deproteinizzata di riferimento (DBBM). Sei mesi dopo l'innesto, la variazione ossea media in larghezza e altezza è stata rispettivamente -1.78% e 1.35% per creos syntogain (n=42) e -2.16% e 2.99% per la DBBM di riferimento (n=41). Le differenze tra i due materiali non sono state statisticamente significative. Il torque medio di inserimento dell'impianto era di 36.2 Ncm nei siti rigenerati con creos syntogain e 35.1 Ncm nei siti rigenerati con la DBBM di riferimento. Per creos syntogain, il 71.1% degli impianti è stato posizionato con un torque di inserimento superiore a 35 Ncm e il 62.8% per la DBBM di riferimento.
L'osso è stabile e mantiene il volume del difetto.2 Rispetto al prodotto di riferimento (DBBM), non è stata osservata alcuna differenza statisticamente significativa nella variazione dimensionale verticale e vestibolare.15
Istruzioni per l'uso creos syntogain
Informazioni importanti e istruzioni per creos syntogain.
Domande su creos syntogain?
Per ulteriori informazioni, maggiori dettagli o domande specifiche su creos syntogain, clicca sul collegamento riportato di seguito.
Quando si utilizza creos syntogain?
La soluzione consente di trattare indicazioni dalle più comuni alle più impegnative.
Tra le altre indicazioni rientrano:
Innesto crestale verticale e orizzontale
Deiscenze dell'osso e fenestrazioni attorno agli impianti

Trova un corso dedicato alla gestione dei tessuti duri e molli
Bibliografia
Per le informazioni complete relative alle prescrizioni, tra cui indicazioni, controindicazioni, avvertenze e precauzioni, consultare le Istruzioni per l'uso.
1. Hoornaert A, Maazouz Y, Pastorino D, et al. Vertical Bone Regeneration with Synthetic Biomimetic Calcium Phosphate onto the Calvaria of Rats. Tissue Eng Part C Methods. 2019 Jan;25(1):1-11. doi: 10.1089/ten.TEC.2018.0260. PMID: 30501579.
2. Raymond Y, Pastorino D, Ginebreda I, et al. Computed tomography and histological evaluation of xenogenic and biomimetic bone grafts in three-wall alveolar defects in minipigs. Clin Oral Investig. 2021 Dec;25(12):6695-6706. doi: 10.1007/s00784-021-03956-y. Epub 2021 May 1. PMID:33931811.
3. Dati in archivio: Granules handling Voice of Customer from 2017-2018 + GKEM Handling Questionnaires Results from 2022.
4. Dati in archivio: Milestone 2 report (chapter 2.5.1)
5. Henkel KO, Gerber T, Lenz S, Gundlach KK, Bienengräber V. Macroscopical, histological, and morphometric studies of porous bone-replacement materials in minipigs 8 months after implantation. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006 Nov;102(5):606-13. doi: 10.1016/j.tripleo.2005.10.034. Epub 2006 May 19. PMID: 17052636.
6. Weibrich G, Trettin R, Gnoth SH, et al. Bestimmung der Größe der spezifischen Oberfläche von Knochenersatzmaterialien mittels Gasadsorption. (Alternate title: Analysis of the size of the specific surface area of bone regeneration materials by gas adsorption). Mund Kiefer GesichtsChir (2000) 4:148-152 Springer-Verlag 2000.
7. Barba A, Diez-Escudero A, Espanol M, et al. Impact of biomimicry in the design of osteoinductive bone substitutes: nanoscale matters. ACS Appl. Mater. Interfaces 2019. DOI:10.1021/acsami.8b20749.
8. Dati in archivio: Mimetis XRD analysis report using the RIR quantification method. Medical device composition certificate.
9. Barba A, Diez-Escudero A, Maazouz Y, et al. Osteoinduction by foamed and 3D-printed calcium phosphate scaffolds: effect of nanostructure and pore architecture. ACS Appl. Mater. Interfaces 2017.DOI:10.1021/acsami.7b14175.
10. Sadowska JM, Guillem-Marti J, Montufar EB, Espanol M, Ginebra MP. * Biomimetic Versus Sintered Calcium Phosphates: The In Vitro Behavior of Osteoblasts and Mesenchymal Stem Cells. Tissue Eng Part A. 2017 Dec;23(23-24):1297-1309. doi: 10.1089/ten.TEA.2016.0406. Epub 2017 Feb 21. PMID: 28107811.
11. Dati in archivio: Milestone 2 study (page 18)
12. Ginebra MP, Espanol M, Maazouz Y, Bergez V, Pastorino D. Bioceramics and bone healing. EFORT Open Rev 2018;3 DOI: 10.1302/2058-5241.3.170056.
13. Dati in archivio: Clinical cases from 2022.
14. Rufino Senra M, de Fátima Vieira Marques M. Synthetic Polymeric Materials for Bone Replacement. J. Compos. Sci. 2020,4, 191;doi:10.3390/jcs4040191.
15. Ginebra Cairó I., Roig Cayón M., Velasco-Ortega E. et al., Biomimetic synthetic bone graft in alveolar ridge preservation: 1-year RCT results, Abstract N°EAO-647 EAO Geneva 2022.